Vertex社がPovetaciceptのグローバル第Ⅲ相臨床試験であるRAINIER試験の中間解析結果を発表
小野薬品工業株式会社(本社:大阪市中央区、代表取締役社長:滝野 十一、以下「当社」)は、米国時間2026年3月9日に、Vertex Pharmaceuticals Incorporated(本社:米国、マサチューセッツ州 ボストン、最高経営責任者: Reshma Kewalramani, M.D.、以下「Vertex社」)が、povetaciceptの第Ⅲ相臨床試験RAINIER試験におけるプレスリリースを発出したことをお知らせします。
本リリースの内容については、Vertex社の英語原文のプレスリリースを和文抄訳として提供するものであり、解釈に相違がある場合は英語原文が優先されます。
英語原文のプレスリリースは、https://news.vrtx.com/ をご覧ください。
当社とVertex社との提携:
当社は2025年6月20日にVertex社とライセンス契約を締結(詳細は こちら を参照)し、povetaciceptについて日本、韓国で独占的に開発・商業化する権利を取得しており、Vertex社によってIgA腎症、原発性膜性腎症を含む複数の重篤なB細胞介在性疾患の治療薬として開発が進められています。
(以下、和文抄訳)
Vertex社、Povetaciceptの第Ⅲ相臨床試験(RAINIER試験)の
36週における中間解析結果で、成人のIgA腎症患者に対して
主要評価項目とすべての副次的評価項目で良好な結果が得られたことを発表
- 主要評価項目である24時間尿タンパク/クレアチニン比(UPCR)がベースラインと比較して52.0%減少し、プラセボ群と比較して統計的有意かつ臨床的意義のある49.8%減少を達成(P<0.0001)
- 1つ目の副次的評価項目であるガラクトース欠損型異常糖鎖IgA1(Gd-IgA1)がベースラインと比較して77.4%減少し、プラセボと比較して統計的有意かつ臨床的意義のある79.3%減少(P<0.0001)でした。2つ目の副次的評価項目である血尿は、povetaciceptを投与した85.1%の患者で改善し、プラセボと比較して統計的有意かつ臨床的意義のある61.7%の改善(P<0.0001)を達成
- Povetaciceptは、全般的に安全かつ忍容性は良好
- Vertex社は米国迅速承認に向けた生物製剤承認申請(BLA)を3月末までに完了
Vertex Pharmaceuticals Incorporated(Nasdaq: VRTX、本社:ボストン)は、本日(3月9日)、IgA腎症(IgAN)を対象としたBAFF (B cell activating factor)およびAPRIL(a proliferation inducing ligand)に対するデュアル阻害剤として開発中の遺伝子組換え融合タンパク質であるpovetaciceptにおける進行中のグローバル第Ⅲ相RAINIER試験で、事前に設定した36週時点の中間解析から良好なデータが得られたことを発表しました。このプレスリリース全文はこちらをご覧ください:
https://www.businesswire.com/news/home/20260309179428/en/
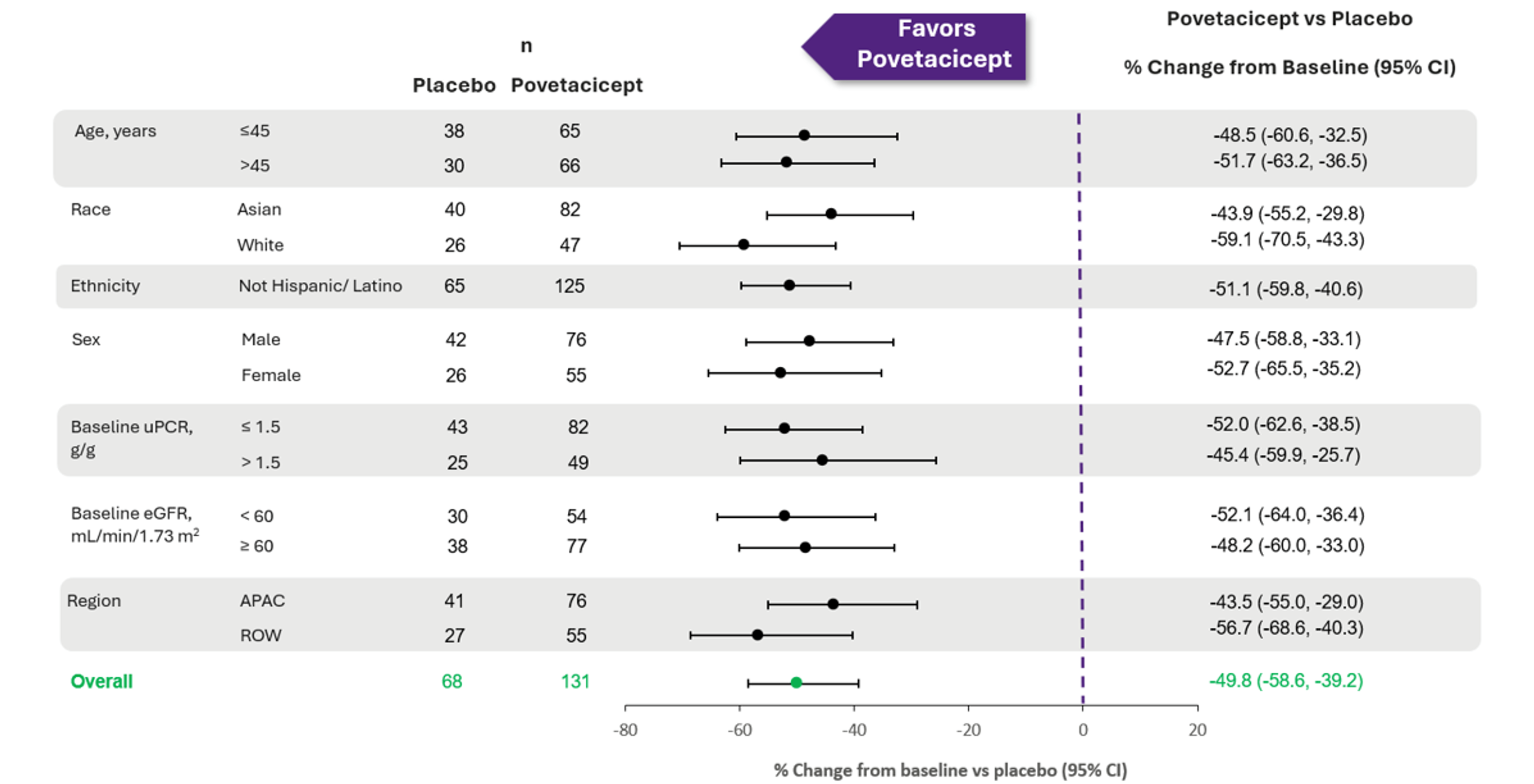
本試験は主要評価項目を達成しました。中間解析対象集団において、povetaciceptを投与された患者は、36週時点で尿中タンパク/クレアチニン比(UPCR)がベースラインから52.0%減少し、プラセボ群と比較して統計的に有意かつ臨床的に意義のある49.8%のUPCR減少が認められました(P<0.0001)。タンパク尿の減少は、事前に規定したすべての患者集団で一貫して認められました。
また、本試験は副次評価項目も達成しました。1つ目の副次的評価項目であるガラクトース欠損型異常糖鎖IgA1(Gd-IgA1)は、povetaciceptを投与された患者がベースラインから77.4%減少し、プラセボ群では9.1%増加しており、プラセボ群と比較して79.3%の減少となりました(P<0.0001)。2つ目の副次的評価項目の血尿では、ベースラインで血尿があった患者のうち、povetacicept投与群では85.1%の患者で血尿が消失し、プラセボ群では23.4%であり、プラセボ群と比較して61.7%の血尿消失という有意な結果が認められました(P<0.0001)。
Povetaciceptは、全般的に安全性が高く、忍容性が良好でした。有害事象の大部分は軽度から中等度でした。Povetaciceptに関連する重篤な有害事象はなく、試験中の死亡例もありませんでした。免疫力が低下した際に発症しやすい感染もなく、中止もありませんでした。当初の予想通り、抗薬物抗体(ADAs)が認められましたが、これらのADAsは有効性やリスクプロファイルに影響を与えませんでした。
中間解析対象集団において、すべての理由による治療中止率は、プラセボ群で8.8%、povetacicept群で3.8%でした。また、すべての理由により試験中止した率は、プラセボ群で1.5%、povetacicept群で0.8%でした。
Vertex社の最高経営責任者(CEO)兼社長であるReshma Kewalramani(M.D., FASN)は次のように述べています。「IgANを対象とした第Ⅲ相RAINIER試験の36週中間解析結果は非常に注目すべきものです。Povetaciceptは、その臨床プロファイル、投与量および利便性、幅広い適応可能性により、ベストインクラスの治療薬となる可能性を示しており、嚢胞性線維症、血液疾患、急性疼痛に続いて腎臓領域をVertex社の第4のフランチャイズとして確立していきます。腎臓専門医として、povetaciceptによる迅速かつ深く持続的な奏効とすべての患者集団で一貫した効果が認められていることに感銘を受けています。これらの結果はIgAN患者にとって重要であり、povetaciceptの“パイプライン・イン・ア・プロダクト”という可能性の実現に一歩近づくものです。患者さんと試験担当医師の皆様には、RAINIER試験を既存のIgANを対象とする試験の中で最大規模かつ最速の患者登録達成に協力いただいたことに感謝します。」
試験デザインと有効性について
RAINIER試験は、povetacicept 80mgを4週間ごとに皮下投与し、標準治療に加えてプラセボと比較する、グローバル第Ⅲ相無作為化二重盲検プラセボ対照試験です。
本試験では合計605名の患者が無作為に割り付けられ、主要解析集団には557名(うち中間解析対象集団は199名)、探索解析集団には48名が含まれています。これらの患者は、腎疾患進行リスクのある実臨床のIgAN患者の特徴を反映している患者群です。主要解析集団におけるIgAN診断から無作為化までの中央値は約3.8年であり、試験参加者の多くが標準治療を受けていました。具体的には、97.8%の患者がアンジオテンシン変換酵素阻害薬(ACE阻害薬)またはアンジオテンシンII受容体拮抗薬(ARB)を使用しており、67.7%の患者ではSGLT2阻害薬を使用していました。SGLT2阻害薬の使用していた患者は最近実施されたIgAN試験の中で最も高い割合となっています。
中間解析における本試験の主要評価項目は、24時間尿中タンパク/クレアチニン比(UPCR)のベースラインからの変化率です。2つの副次評価項目は、ガラクトース欠損型異常糖鎖IgA1(Gd-IgA1)のベースラインからの変化率と、血尿が消失した患者の割合であり、いずれも36週時点で評価します。今回の中間解析における探索的評価項目には、24時間UPCRが0.5g/g未満の患者の割合が含まれており、これは最新の腎疾患ガイドライン(KDIGO)に準拠しています。
| プラセボ N=68 |
Povetacicept N=131 |
|
|---|---|---|
| 主要評価項目 | ||
| ベースラインからの24時間UPCRの変化率(%) | -4.3 | -52.0 |
| プラセボと比較した変化率(%) | -49.8 | |
| 対プラセボにおけるP値 a | <0.0001 | |
| 副次的評価項目::Gd-IgA1 | ||
| ベースラインからのGd-IgA1の変化率(%) | +9.1 | -77.4 |
| プラセボと比較した変化率(%) | -79.3 | |
| P value vs. placebo a | <0.0001 | |
| 副次的評価項目: 血尿 b | ||
| 消失が認められた患者の割合(%) | 23.4 | 85.1 |
| プラセボ群と比較した改善(消失)患者の割合の差(%) | 61.7 | |
| 対プラセボにおけるP値 a | <0.0001 | |
| 探索的評価項目 | ||
| 24時間尿中タンパク/クレアチニン比(UPCR) <0.5 g/g (%) | 6.2 | 42.2 |
a Two-sided P value(両側検定によるp値)
b 治療開始時に血尿があった患者での血尿消失(プラセボ群N=36、povetacicept 群N=67)
安全性について
Povetaciceptは、全般的に安全性が高く、忍容性は良好でした。以下のデータは、主要解析集団(557名)におけるものであり、povetacicept群の平均治療期間は33.7週、プラセボ群は33.4週でした。
| プラセボ N=185 n (%) |
Povetacicept N=372 n (%) |
|
|---|---|---|
| 有害事象が発現した患者数 | 145 (78.4) | 279 (75.0) |
| いずれかの群で10%以上発現した有害事象 | ||
| 上気道感染 | 21 (11.4) | 68 (18.3) |
| 咽頭炎 | 23 (12.4) | 36 (9.7) |
| 注射部位反応 a | 4 (2.2) | 54 (14.5) |
a 注射部位反応(ISR)は、事前に規定されたPreferred Terms(例:注射部位反応、注射部位紅斑など)を用いて特定されました。すべてのISRは重篤ではなく、軽度または中等度でした。
重篤な有害事象は、プラセボ群では4.3%(185人中8人)、povetacicept群では3.0%(372人中11人)に発生しました。感染による重篤な有害事象の発生率は、両群とも0.5%でした。
今後の動向
米国食品医薬品局(FDA)は、IgANに対するpovetaciceptの生物製剤承認申請(BLA)について、ローリングレビューを認めています。そのため、Vertex社はすでに複数のモジュールを提出しており、迅速承認の可能性に向けて、3月末までにBLAの全提出を完了する予定です。すでに公表 している通り、Vertex社は優先審査バウチャーを活用し、povetaciceptのBLA審査期間を通常の10か月から6か月に短縮しています。
PovetaciceptがFDAに承認された場合、Vertex社は0.5mL未満の低容量の皮下注射用オートインジェクターを用い、4週間ごとに自宅で投与できる剤型でpovetaciceptを発売する計画です。
RAINIER試験は引き続き二重盲検下で実施され、最終解析は2年間の治療後に行われます。主要評価項目は104週までの推定糸球体濾過率(eGFR)となります。RAINIER試験の全患者登録完了の発表は2025年11月にしています。
Povetaciceptについて
Povetaciceptは、BAFF(B cell activating factor)およびAPRIL(a proliferation inducing ligand)に対するデュアル拮抗薬です。BAFFおよびAPRILは、B細胞の活性化、分化および生存を促進し、複数の自己免疫疾患の病態進展に重要な役割を果たしており、povetaciceptはBAFFおよびAPRILを阻害することでB細胞の働きを制御します。Povetaciceptは遺伝子改変TACI(transmembrane activator and CAML interactor)ドメインからなり、前臨床試験において、他のAPRIL阻害薬やBAFF阻害薬の単剤投与、またはBAFF+APRIL阻害薬と比較して高い結合親和性および効果、薬物動態、または組織分布を示します。
Povetaciceptは、IgANの治療薬としてFDAの Breakthrough Therapy 指定を受けています。また、昨年末の発表 の通り、FDAはローリングレビューも認めています。
Povetaciceptは、複数の腎疾患を対象とした主要試験において、唯一のBAFFおよびAPRILのデュアル阻害剤です。Povetaciceptの適応拡大も進行中で、原発性膜性腎症(pMN)を対象とした第2/3相OLYMPUS試験が進行中であり、全身型重症筋無力症(gMG)を対象としたETNA第2相試験も2026年前半に開始予定です。
Povetaciceptは開発中の治験薬であり、いずれの国や地域でも承認されていません。
IgA Nephropathy (IgAN) について
IgA腎症は、制御不能の自己反応性B細胞活性化によって引き起こされる重篤で進行性、かつ生命を脅かす腎臓病で、原発性糸球体腎炎の最も一般的な原因であり、米国、欧州で約33万人が罹患しており、世界で150万人以上います。IgA腎症は、免疫グロブリンとガラクトース欠損型糖鎖異常IgA1(Gd-IgA1)からなる免疫複合体が腎糸球体メサンギウムに沈着することで発症し、腎障害と線維化を引き起こします。最大72%のIgA腎症患者は20年以内に末期腎不全や死に進行します。
RAINIER試験について
RAINIER試験(NCT06564142)は、標準治療に加えてpovetacicept 80 mgを4週間ごとに皮下投与する群とプラセボを投与する群を比較するグローバル第III相無作為化プラセボ対照ピボタル試験です。本試験では合計605名の患者が無作為化され、そのうち557名が主要解析集団、48名が探索的解析集団に割り付けられました。両集団の組み入れ基準は同じですが、主要解析集団ではeGFRが30 mL/min/1.73m²以上、探索的集団では20以上30未満と定められていました。
本試験は、あらかじめ定められた人数の患者が36週間の治療を完了した時点で中間解析を実施するよう設計されていました。中間解析における有効性評価の対象は199名で、これは主要解析集団の一部です。中間解析時の主要評価項目は、36週時点における24時間UPCRのベースラインからの変化率であり、偶然による偽陽性が増えないように有意水準を調整した2つの副次評価項目は、同じく36週時点でのGd-IgA1のベースラインからの変化率と、ベースライン時に血尿があった患者における血尿消失の割合です。主要集団(557名)は安全性評価の主な対象集団となります。最終解析は2年間の治療後に実施され、主要評価項目は104週までのeGFRです。
RAINIER試験は、IgANを対象とした試験としては最大規模であり、同時期に実施された他のIgAN試験と比べて最も早く患者登録を完了しました。
Vertexについて
Vertex社は、重篤な疾患に対する革新的な医薬品を創出するための科学的イノベーションに投資するグローバルバイオテクノロジー企業です。Vertexは、嚢胞性線維症、鎌状赤血球症、輸血依存性ベータサラセミア、急性痛に対する複数の承認薬剤を有しており、これら疾患に対する臨床開発や研究プログラムを推進し続けています。また、Vertexは、神経障害性疼痛、APOL1介在性腎疾患、IgA腎症、原発性膜性腎症、常染色体優性多発性嚢胞腎、1型糖尿病、筋強直性ジストロフィー1型を含むヒト生物学的な原因について深い洞察が得られている他の重篤な疾患において幅広いモダリティを対象とした強固な開発パイプラインを有しています。
Vertex社は1989年に設立され、ボストンにグローバル本社を、ロンドンに国際本部を有しています。さらに、北米、欧州、オーストラリア、中南米および中東に研究開発拠点および営業拠点を有しています。Vertexは、サイエンス誌の「Top Employers list」に16年連続でランクインし、フォーチュン誌の「100 Best Companies to Work For」にも選出されるなど、業界トップクラスの働きがいのある企業として高い評価を得ています。Vertexに関する最新情報やVertex社のイノベーションの歴史を更に知りたい方は、www.vrtx.com をご覧いただくか、LinkedIn 、Facebook 、Instagram 、YouTube および X をフォローしてください。
